“Genes genocidas”: el riesgo de acabar con una especie para que otra no se extinga

El mercado en torno a la herramienta de edición genética CRISPR moverá más de 5.500 millones de dólares en 2021, según las estimaciones más recientes. Una de las empresas que impulsarán y se beneficiarán de esta tecnología será Monsanto. La controvertida multinacional anunciaba recientemente que ha adquirido la licencia para usarla con fines agrícolas tras llegar a un acuerdo con el Instituto Broad, un centro de investigación perteneciente a la Universidad de Harvard y el MIT.
Sin embargo, el permiso viene con una clara restricción: la empresa no podrá utilizar CRISPR para aplicar técnicas de modificación genética dirigida, aquellas alteraciones del ADN destinadas a fomentar o suprimir la expresión de ciertos genes en poblaciones de una especie para perpetuar un rasgo entre los individuos.
Este método despierta reticencias también entre algunos expertos de la Unión Internacional para la Conservación de la Naturaleza (UICN), reunidos recientemente en un congreso mundial celebrado en Hawái. Han emitido una petición formal para que se estudien detenidamente sus riesgos e “impactos potenciales” en la biodiversidad y se elaboren guías que regulen su uso antes de su aplicación masiva.
Lo mismo demanda un comité científico conjunto de la Academia Nacional de Ciencias, la de Ingeniería y la de Medicina estadounidenses que este verano publicaba el informe ‘La genética dirigida en el horizonte’. Sus autores advierten de que “las pruebas de concepto realizadas hasta la fecha en unos pocos estudios de laboratorio no son suficientes para justificar la decisión de liberar organismos modificados mediante genética dirigida al medio ambiente”.
Los posibles efectos negativos se enmarcan en los ámbitos social y ecológico, según explica a HojaDeRouter.com Kevin Esvelt, líder del laboratorio ‘Sculpting Evolution’ del MIT. Por una parte, “la liberación accidental o deliberada de un precursor genético sin el apoyo de la sociedad podría mellar la confianza pública en científicos y gobiernos […] Esto podría paralizar las aplicaciones de genética dirigida que pueden salvar millones de vidas y la existencia de algunas especies”, indica Esvelt.
Por otra, “no conocemos muy bien cómo funcionan los ecosistemas, por lo que es difícil predecir qué podría ir mal”, admite el estadounidense. “La mejor manera de averiguarlo es liberar organismos con la alteración pero sin un sistema de genética dirigida para estudiar su impacto ambiental en un área”.
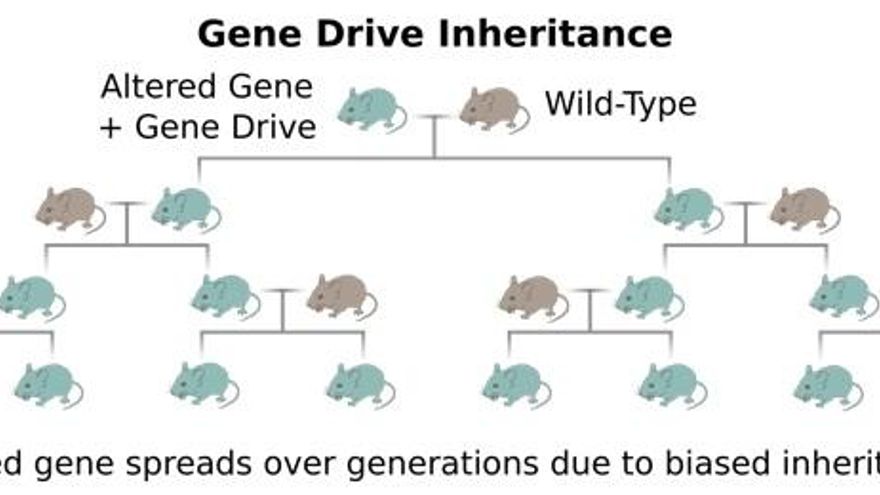
Una de las últimas investigaciones en la materia se ha realizado en la Universidad de California. Allí han creado mosquitos modificados genéticamente para resistir al parásito de la malaria y, por tanto, incapaces de transmitirla. Al reproducirse con otros de su especie, pasan sus genes resistentes a la descendencia, por lo que perpetuarían el rasgo en una población y, teóricamente, podrían llegar a acabar con el contagio a humanos. “Si se aplicara con éxito en la naturaleza, la estrategia podría incluso erradicar la enfermedad”, sugerían los investigadores en su artículo, publicado en la revista Science.
Utilizaron la técnica mejorada CRISPR/Cas9, “mucho más dirigida, mucho más concreta, que permite ir exactamente a un lugar del genoma y alterar un gen concreto”, explica Antoni Barbadilla, experto en genética de la Universidad de Barcelona (UB). Al contrario de lo que ocurre en transgénesis, el método no se usa para introducir genes de otro organismo, sino que permite modificar los del mismo individuo, por ejemplo, inactivándolos para que no se expresen.
Sin embargo, para ambientalistas como la famosa Jane Goodall, la genética dirigida aún “no se ha puesto a prueba para estimar consecuencias accidentales ni se han evaluado totalmente sus implicaciones éticas y sociales”. Así lo advierte en una carta que han firmado también expertos en bioética y derecho ambiental. En la misiva solicitan directamente que una técnica “potencialmente peligrosa” no sea utilizada en conservación y se oponen a liberar al medio lo que han denominado “genes genocidas”, que podrían utilizarse para erradicar especies difundiendo genes de infertilidad con el objetivo de salvar a otras.
Una oportunidad para evitar la extinción
Aunque nadie habla de terminar con especies enteras, “los sistemas de genética dirigida basados en la supresión podrían reducir la fertilidad de especies invasoras y eliminarlas de ecosistemas sensibles como los de las islas”, señala Esvelt. Un equipo de científicos de la Universidad de Hawái, liderados por el biólogo Floyd Reed, consideran utilizar esta estrategia con poblaciones de mosquitos del género ‘Culex’, transmisores de la malaria aviar, que causan graves estragos en el archipiélago. La enfermedad diseminada por estos insectos supone una importante amenaza para aves como los mieleros hawaianos, una especie endémica en peligro de extinción.
Reed y su equipo estudian cómo modificar genéticamente a los insectos para que no puedan transmitir la malaria o reproducirse, pero basándose en una estrategia conocida como subdominancia. La idea consiste en liberar individuos alterados al medio hasta que superen el 50 % de la población total, creando una situación de equilibrio inestable que podría revertirse. Aunque con otros métodos, en Nueva Zelanda se han propuesto acabar con las poblaciones de especies invasoras de ratas, comadrejas y armiños, que matan a millones de aves todos los años.

Esvelt explica que, al contrario de lo que creen algunos grupos conservacionistas, la genética dirigida no podría llevar a una especie a la extinción por “razones técnicas”. Para conseguirlo habría que emplear “múltiples sistemas de genética dirigida basados en supresión, monitorizar el proceso activamente, esforzarse para aniquilar las últimas reservas y prescindir de cualquier programa de conservación”, explica. “No hay manera de extinguir una especie con técnicas de deriva genética a no ser que el mundo entero estuviera de acuerdo”.
No obstante, el estadounidense admite que es inseguro crear herramientas de genética dirigida globales, es decir, aquellas que podrían extenderse indefinidamente en la naturaleza. “Un solo accidente en el laboratorio en el que un organismo escapara permitiría que se difundiera y afectara a los ecosistemas y a las vidas de la gente que no lo ha consentido”, dice Esvelt. Según el informe de las academias científicas estadounidenses, cualquier grupo de investigación centrado en esta área debe hacer públicos los objetivos y líneas de su trabajo.
Por su parte, Barbadilla ve totalmente necesario estimar y controlar las posibles implicaciones y no dejar nada al azar, pero opina que un exceso de cautela frena el desarrollo científico. Una postura ante la que otros tienen sus reservas. “Hay mucha sensibilidad en este tema y se han creado grupos contrarios muy activos que lo encuentran muy arriesgado”, explica el español.
¿Equilibrio o desequilibrio?
“El problema es que asumimos que la naturaleza está equilibrada y que nosotros lo rompemos”, recalca el investigador de la UB. En el caso de Hawái, “los mosquitos están produciendo un desequilibrio ecológico que podríamos corregir”, señala, aunque “no sabemos el efecto en cascada que podría ocasionar”.
“Hay especies con mucha importancia en una red trófica, cuya alteración lo cambia todo, mientras que hay otras que prácticamente no influyen”, añade. Por eso, en su opinión, “habría que saber exactamente cuál es el papel de esa población” antes de poner en marcha una estrategia. No obstante, Barbadilla cree que el uso de una técnica tan precisa como CRISPR/Cas9 y el hecho de que el ADN alterado pertenezca al propio individuo son factores que reducen el peligro.
En la manipulación basada en el traspaso de elementos genéticos de una especie a otra, “siempre se ha criticado que podría cambiarse el genoma, expandirse la modificación y, potencialmente, podría hacer mucho daño”, recuerda el investigador. Sin embargo, en genética dirigida “no se añade nada nuevo, solo alteras algo que ya estaba presente”. Según el científico, “la inactivación de un gen es una mutación como las que sufrimos constantemente todos los organismos en la naturaleza, por lo que el riesgo potencial sería menor”.
Debido a esta diferencia, “para muchos, no debería aplicarse la misma legislación que en transgénesis, sino que debería ser algo más sencillo e inmediato”, señala Barbadilla, por lo que también hay abierto un debate en el ámbito normativo. Además, la herramienta de edición genética CRISPR arrastra otra polémica legal: pese a la adquisición de la licencia de uso por parte de diferentes empresas, sigue sin esclarecerse si la patente es propiedad del Instituto Broad o de la Universidad de California en Berkeley, donde se utilizó por primera vez en 2012 para modificar el ADN de bacterias.
En opinión de Barbadilla, ninguna de estas controversias debería suponer un freno al avance y desarrollo de la técnica. “Cada adelanto tecnológico y científico realmente potente tiene sus riesgos y hay que considerarlos, pero no podemos permitir que nos paralicen”, sentencia el español.
--------------
Las imágenes de este artículo son propiedad, por orden de aparición, dewoodleywonderworks, MIT y CRISPRLab/NCSU




